Biofilme sind komplexe mikrobiologische Gemeinschaften aus Bakterien und anderen Mikroorganismen, die sich in einer selbst produzierten, schleimigen Matrix ansiedeln. Diese extrazelluläre Matrix schützt die Mikroben nicht nur vor dem Immunsystem des Wirts, sondern auch vor antimikrobiellen Wirkstoffen wie Antibiotika. Biofilme kommunizieren über chemische Signale („Quorum Sensing“) und gehen in einen sesshaften Lebensmodus über, der zu chronischen Infektionen führt und die Wundheilung erheblich verzögert oder verhindert. Allein in Deutschland stehen schätzungsweise rund 100.000 Infektionen pro Jahr im Zusammenhang mit Biofilmen – etwa bei Implantaten, Wunden und anderen medizinischen Kontexten.
Konventionelle Strategien in der Biofilm-orientierten Wundversorgung
Im klinischen Alltag haben sich mehrere Ansätze etabliert, um die Präsenz von Biofilmen bei chronischen und schlecht heilenden Wunden zu adressieren:
1. Wundreinigung und Débridement
Der erste Schritt jeglicher Biofilm-orientierter Therapie besteht in der Vorbereitung des Wundbetts. Mechanisches oder chirurgisches Débridement entfernt nekrotisches Gewebe und Beläge, die als Nährboden oder Schutz für mikrobielles Material dienen, und erleichtert so den Zugang zu tiefer liegenden Strukturen. International anerkannte Protokolle betrachten Débridement als essenziellen Schritt zur Disruption der Biofilm-Matrix. Wichtig ist dabei zu betonen, dass selbst nach konsequentem Débridement oft nicht alle Biofilmreste vollständig entfernt werden; die Mikroorganismen können sich innerhalb weniger Stunden (teilweise <24 h) wieder reorganisieren und einen neuen Schutzfilm bilden.
2. Antiseptische Reinigung und Antimikrobielle Therapien
Nach Débridement ist die Anwendung topischer antimikrobieller Mittel ein etablierter Standard. Häufig eingesetzt werden Antiseptika wie Octenidin, Polyhexamethylen-Biguanid (PHMB) und Povidon-Iod, die in Studien Biofilm-assoziierte Mikroorganismen reduzieren können. Systemische Antibiotikatherapie allein ist bei Biofilmbesiedelung oft ineffektiv, da Biofilm-Matrix und metabolisch inaktive Bakterienzellen den Antibiotika-Penetrationsweg blockieren und systemische Konzentrationen am Wundort nicht ausreichend sind.
3. Antimikrobielle Wundauflagen
Spezielle antimikrobielle Wundauflagen – z. B. mit Silber, PHMB oder kombinierten Wirkstoffen – werden genutzt, um die mikrobielle Belastung lokal zu reduzieren und die Neubildung von Biofilmen zu hemmen. Diese Auflagen sind besonders sinnvoll nach Débridement, da sie die verbliebenen Mikroorganismen adressieren und das Risiko der raschen Neuformierung eines Biofilms mindern.
Neuere und innovative Anti-Biofilm-Strategien
Während die klassische Behandlung die meisten Standardfälle abdeckt, zeigen aktuelle Studien, dass konventionelle Maßnahmen allein häufig nicht ausreichen. Neue Ansätze zielen darauf ab, Biofilm gezielter zu stören oder die Bildung frühzeitig zu verhindern.
1. Enzymatische Biofilm-Disruption
Biologisch aktive Enzyme wie Dispersin B, DNase I oder alpha-Amylase können die extrazelluläre Matrix gezielt abbauen und die strukturelle Integrität des Biofilms stören. Dadurch werden Bakterien wieder zugänglicher für antibakterielle Therapien.
Vorteile:
- Zielt direkt auf die Matrix ab
- Kann die Wirksamkeit anderer Therapien (z. B. Antibiotika) verbessern
Kritikpunkte:
- Noch überwiegend in experimentellen Studien
- Nicht flächendeckend klinisch implementiert
2. Quorum-Sensing-Inhibitoren
Die Kommunikation zwischen Biofilm-Bakterien („Quorum Sensing“) steuert deren Koordination und Widerstandsfähigkeit. Moleküle, die diese Signalketten blockieren, könnten verhindern, dass sich Biofilme überhaupt stabil bilden oder erhalten bleiben. Forschende am HZI arbeiten beispielsweise an Substanzen, die Lektine blockieren – Protein-Bindungsstellen, welche in der Biofilm-Matrix eine strukturelle Rolle spielen.
Vorteile:
- Greift bereits in der Frühphase der Biofilmbildung ein
Kritikpunkte:
- Klinische Daten zur Wirksamkeit beim Menschen sind derzeit begrenzt
3. Nanotechnologische und physikalische Ansätze
Neue Dressings und Materialien, etwa nanopartikelbasierte Systeme oder „smart dressings“, die antimikrobielle Wirkstoffe bedarfsorientiert freisetzen, werden aktuell erforscht. Diese können lokal höhere Wirkstoffkonzentrationen erreichen oder Biofilme materialphysikalisch stören.
Vorteile:
- Potenziell größere Effektivität
- Möglichkeit multidimensionaler Wirkmechanismen
Kritikpunkte:
- Kosten und Langzeitdaten sind oft noch unzureichend
4. Raponic™ Technologie
Die Raponic™-Technologie basiert auf einer weiterentwickelten PHMB-Formulierung, die Mikroorganismen in der Wunde länger hemmen, die Wundheilung unterstützen und gleichzeitig Gewebe schonen soll. Klinische Daten zeigen positive Effekte auf Heilung und Schmerzlinderung. (wounds-uk.com)
Vorteile:
- Längere Wirkdauer, ermöglicht längere Intervalle zwischen Verbandwechseln
- Breite antimikrobielle Wirkung
- Verbesserte Verträglichkeit und Schmerzlinderung
- Unterstützt Antibiotic Stewardship
Kritikpunkte:
- Spezifische Biofilm-auflösende Effekte sind noch nicht eindeutig klinisch quantifiziert
- Evidenz basiert teilweise auf herstellerunterstützten Studien
5. Molekulare Adhäsions‑Inhibitoren
Innovative Ansätze zielen darauf ab, die frühen Schritte der Biofilmbildung zu verhindern, indem die bakterielle Haftung blockiert wird. Glykomimetische Inhibitoren, wie sie z. B. gegen das LecA-Lectin von Pseudomonas aeruginosa entwickelt wurden, binden an bakterielle Proteine und stören die initiale Anheftung.
Vorteile:
- Greift sehr früh in die Biofilm-Bildung ein
- Potenziell geringer Selektionsdruck für Resistenzen
- Ergänzt physikalische und chemische Biofilm-Disruptoren
Kritikpunkte:
- Aktuell vorwiegend experimentelle Evidenz
- Klinische Daten fehlen größtenteils
- Spezifität kann je nach Erregerspektrum variieren
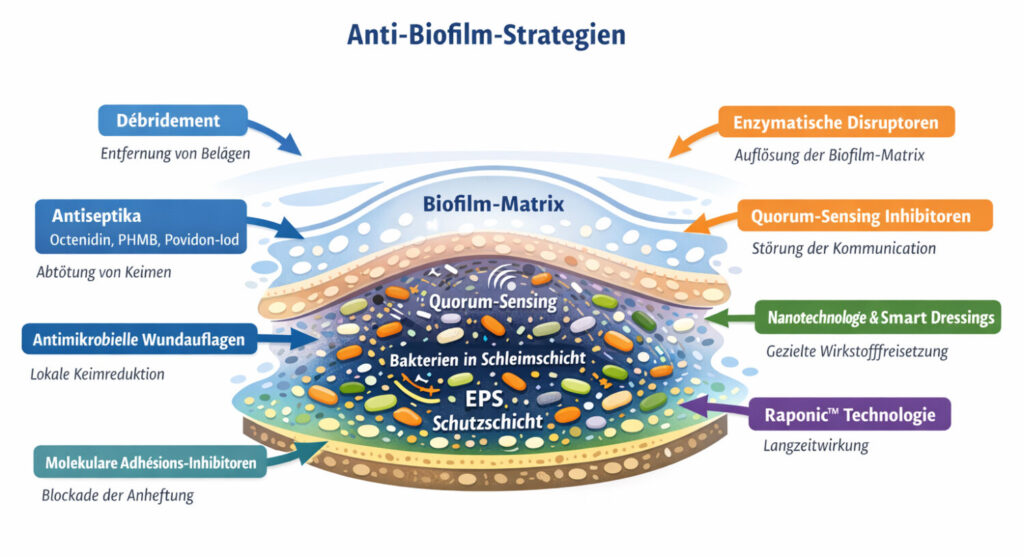
Angriffsmechanismen der Strategien im Überblick:
Die nachfolgende Grafik macht auf einen Blick deutlich, wie Débridement, antiseptische Mittel, antimikrobielle Auflagen, enzymatische Disruptoren, Quorum-Sensing-Inhibitoren, nanotechnologische Dressings, die Raponic™-Technologie und molekulare Adhäsions-Inhibitoren auf unterschiedliche Bereiche der Biofilm-Matrix wirken.
| Strategie | Wirkmechanismus / Angriffsbereich im Biofilm |
|---|---|
| Débridement | Entfernt oberflächliches Material und teilweise Matrix |
| Antiseptische Mittel (Octenidin, PHMB, Povidon-Iod) | Reduziert Mikroorganismen in der Matrix |
| Antimikrobielle Wundauflagen | Lokale Reduktion der mikrobiellen Belastung, hemmt Neubildung |
| Enzymatische Disruptoren (Dispersin B, DNase I) | Löst die extrazelluläre Matrix auf, erhöht Zugänglichkeit |
| Quorum-Sensing-Inhibitoren | Blockiert bakterielle Kommunikation, stört Koordination |
| Nanotechnologische / Smart Dressings | Physikalische Störung + kontrollierte Wirkstofffreisetzung |
| Raponic™ | Verlängerte antimikrobielle Wirkung auf Bakterien |
| Molekulare Adhäsions-Inhibitoren | Verhindert initiale Anheftung an Gewebe |
Kurz gesagt
Biofilme sind ein zentraler Hemmfaktor für die Wundheilung und erfordern einen multidimensionalen Therapieansatz. Die Basis bildet weiterhin die konventionelle Wundversorgung: Débridement, antiseptische Reinigung und antimikrobielle Wundauflagen.
Darüber hinaus bieten neue, gezielte Anti-Biofilm-Strategien vielversprechende Ergänzungen: enzymatische Disruptoren, Quorum-Sensing-Inhibitoren, nanotechnologische Systeme, innovative PHMB-Formulierungen wie die Raponic™-Technologie sowie molekulare Adhäsions-Inhibitoren, die frühe Schritte der Biofilmbildung blockieren.
Die Kombination dieser Ansätze könnte es künftig ermöglichen, Biofilm sowohl frühzeitig zu verhindern als auch bereits etablierte Biofilme wirksam zu bekämpfen. Dies wird die Heilungschancen verbessern und den Komfort für Patienten und Patientinnen erhöhen.
Quellen und Literaturhinweise
- Helmholtz-Zentrum für Infektionsforschung. Biofilme: Ein Leben im Schleim. (helmholtz-hzi.de)
- Wounds International. Autolytic continuous debridement with a focus on biofilm management. (woundsinternational.com)
- Shen A.Z. et al., Biofilms and Chronic Wounds: Pathogenesis and Treatment Options, J Clin Med 2025. (pubmed.ncbi.nlm.nih.gov)
- MDPI. Microbial Biofilms as Barriers to Chronic Wound Healing. (mdpi.com)
- ScienceDirect. Antiseptische Strategien & moderne Wundversorgung. (sciencedirect.com)
- MDPI. Enzymatische Biofilm-Disruption. (mdpi.com)
- Luminwaves. Innovative Approaches in Biofilm Wound Care. (luminwaves.com)
- Angewandte Chemie, DOI: 10.1002/anie.202508864 – Glycomimetic LecA Inhibitors zur Biofilmprävention. (wiley.com)
- Beitragsbild mit Glühbirne: Marco Verch. Lizenz: CC BY 2.0 DE
- Grafik “Anti-Biofilm-Strategien”: Mit Hilfe von KI generiert





